Đặt hai cốc A và B có khối lượng bằng nhau lên 2 đĩa cân thì cân thăng bằng. Cho 10,6 gam Na2CO3 vào cốc A và 5 gam CaCO3 vào cốc B, thêm 20 gam dung dịch H2SO4 9,8% vào cốc A và m gam HCl 18,25% vào cốc B thì cân thăng bằng. Tính m

Những câu hỏi liên quan
3-Cho 2 cốc A,B có cùng khối lượng. Đặt A, B lên hai đĩa cân, cân thăng bằng. Cho vào cốc A 126 gam K2CO3 và vào cốc B 85 gam AgNO3. Thêm vào cốc A 100g dung dịch H2SO4 19,6% và vào cốc B 100 gam dung dịch HCl 36,5%. Hỏi phải thêm bao nhiêu g H2O vào cốc A hay cốc B để cân lập lại thăng bằng
Đặt 2 cốc A, B có khối lượng bằng nhau lên 2 đĩa cân thấy cân thăng bằng. Cho 10,6 gam Na2CO3 vào A và 11,82 gam BaCO3 vào B, sau đó thêm 12 gam dung dịch H2SO4 98% vào A, cân mất nhăng bằng. Nếu thêm từ từ m gam dung dịch HCI 14,6% vào B cho tới khi cân trở lại thăng bằng. Biết các phản ứng xảy ra hoàn toàn. Viết các phương trình phản ứng và tính giá trị của m
Phương trình phản ứng trong cốc A:
Na2CO3 + H2SO4 -> Na2SO4 + H2O + CO2
Phương trình phản ứng trong cốc B:
BaCO3 + HCl -> BaCl2 + H2O + CO2
Ta có thể tính khối lượng của BaCO3 và Na2CO3 như sau:
Khối lượng BaCO3 = 11,82g
Khối lượng Na2CO3 = 10,6g
Để tính khối lượng dung dịch HCl cần thêm vào B, ta sử dụng quy tắc tỉ lệ:
(11,82g BaCO3) : (14,6% HCl) = (m gam BaCO3) : (100% HCl)
Từ đó, ta tính được m gam HCl cần thêm vào B:
m = (11,82g BaCO3) x (100% HCl) / (14,6% HCl) ≈ 80,82g
Vậy giá trị của m là khoảng 80,82 gam.
Đúng 0
Bình luận (3)
Đặt 2 cốc A, B có cùng khối lượng lên 2 đĩa cân thăng bằng. Cho vào cốc A 102 gam chất a) Thêm 100 gam dung dịch HCl 29,2% vào cốc A; 100 gam dung dịch H2SO4 24,5% vào cốc B cho đến khi các phản ứng xảy ra hoàn toàn. Phải thêm bao nhiêu gam nước vào cốc A (hay cốc B) để cân trở lại thăng bằng? b) Sau khi cân đã thăng bằng, lấy ½ lượng dung dịch có trong cốc A cho vào cốc B. Sau phản ứng, phải thêm bao nhiêu gam nước vào cốc A để cân trở lại thăng bằng?
Đọc tiếp
Đặt 2 cốc A, B có cùng khối lượng lên 2 đĩa cân thăng bằng. Cho vào cốc A 102 gam chất
a) Thêm 100 gam dung dịch HCl 29,2% vào cốc A; 100 gam dung dịch H2SO4 24,5% vào cốc B cho đến khi các phản ứng xảy ra hoàn toàn. Phải thêm bao nhiêu gam nước vào cốc A (hay cốc B) để cân trở lại thăng bằng?
b) Sau khi cân đã thăng bằng, lấy ½ lượng dung dịch có trong cốc A cho vào cốc B. Sau phản ứng, phải thêm bao nhiêu gam nước vào cốc A để cân trở lại thăng bằng?
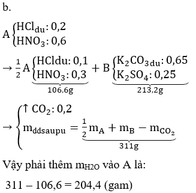
a.
|
|
AgNO3 |
K2CO3 |
| Ban đầu |
0,6 mol; 102 gam |
0,9 mol; 124,2 gam |
| Thêm vào |
→ HCl : 0 , 1 mol ↓ AgCl : 0 , 6 mol |
← H 2 SO 4 : 0 , 25 ↑ CO 2 : 0 , 25 |
| Sau phản ứng |
115,9gam |
213,2 gam |
| Thêm nước |
213,2 – 115,9 = 97,3 gam |
|
Đúng 0
Bình luận (0)
Đặt hai cốc A, B có khối lượng bằng nhau lên 2 đĩa cân, cân ở vị trí thăng bằng. Cho dung dịch HCl vào cốc A; dung dịch H2SO4 loãng vào cốc B. Khối lượng axit được lấy vào 2 cốc bằng nhau sao cho cân vẫn giữ nguyên trạng thái cân bằng. Thêm 7,84 gam Fe vào cốc A; 8,1 gam Al vào cốc B. Sau thí nghiệm, cân có còn ở vị trí thăng bằng không? Giải thích? Biết rằng kim loại trong 2 phản ứng trên đều phản ứng hết.Giúp mình nha
Đọc tiếp
Đặt hai cốc A, B có khối lượng bằng nhau lên 2 đĩa cân, cân ở vị trí thăng bằng. Cho dung dịch HCl vào cốc A; dung dịch H2SO4 loãng vào cốc B. Khối lượng axit được lấy vào 2 cốc bằng nhau sao cho cân vẫn giữ nguyên trạng thái cân bằng. Thêm 7,84 gam Fe vào cốc A; 8,1 gam Al vào cốc B. Sau thí nghiệm, cân có còn ở vị trí thăng bằng không? Giải thích? Biết rằng kim loại trong 2 phản ứng trên đều phản ứng hết.
Giúp mình nha
\(n_{Fe}=\dfrac{7,84}{56}=0,14\left(mol\right);n_{Al}=\dfrac{8,1}{27}=0,3\left(mol\right)\)
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: 0,14 0,14
PTHH: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
'Mol: 0,3 0,45
⇒ Khối lượng đc thêm vào ở cốc A là 7,84-0,14.2=7,56 (g)
Khối lượng đc thêm vào ở cốc B là 8,1-0,45.2=7,2 (g)
⇒ Cốc A nặng hơn cốc B (do khối lượng axit được lấy vào 2 cốc bằng nhau )
Vậy cân ko còn ở vị trí thăng bằng
Đúng 0
Bình luận (0)
Đặt hai cốc A và B có khối lượng bằng nhau lên 2 đĩa cân thì cân thăng bằng. Cho 10,6 gam Na2CO3 vào cốc A và 5 gam CaCO3 vào cốc B, thêm 20 gam dung dịch H2SO4 9,8% vào cốc A và m gam HCl 18,25% vào cốc B thì cân thăng bằng. Tính m
Đặt hai cốc A, B có khối lượng bằng nhau lên 2 đĩa cân, cân ở vị trí thăng bằng. Cho dung dịch HCl vào cốc A; dung dịch H2SO4 loãng vào cốc B. Khối lượng axit được lấy vào 2 cốc bằng nhau sao cho cân vẫn giữ nguyên trạng thái cân bằng. Thêm 7,84 gam Fe vào cốc A; 8,1 gam Al vào cốc B. Sau thí nghiệm, cân có còn ở vị trí thăng bằng không? Giải thích? Biết rằng kim loại trong 2 phản ứng trên đều phản ứng hết.
Đọc tiếp
Đặt hai cốc A, B có khối lượng bằng nhau lên 2 đĩa cân, cân ở vị trí thăng bằng. Cho dung dịch HCl vào cốc A; dung dịch H2SO4 loãng vào cốc B. Khối lượng axit được lấy vào 2 cốc bằng nhau sao cho cân vẫn giữ nguyên trạng thái cân bằng. Thêm 7,84 gam Fe vào cốc A; 8,1 gam Al vào cốc B. Sau thí nghiệm, cân có còn ở vị trí thăng bằng không? Giải thích? Biết rằng kim loại trong 2 phản ứng trên đều phản ứng hết.
HYJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJJ
Cho a gam CaCO3 vào cốc A và a gam MgCO3 vào cốc B rồi đặt hai cốc lên cân thì thấy khối lượng hai cốc bằng nhau. Cho tiếp vào mỗi cốc V ml dung dịch HCl 1M, sau khi các phản ứng xảy ra hoàn toàn thì cốc nào có khối lượng lớn hơn? Giải thích.
- Trường hợp 1: HCL dư
Có: n CaCO3 = \(\dfrac{a}{100}\left(mol\right)\)
n MgCO3 = \(\dfrac{a}{84}\left(mol\right)\)
PTHH
CaCO3 + 2HCl \(\rightarrow\) CaCL2 + CO2 + H2O
\(\dfrac{a}{100}\)--------------------------------\(\dfrac{a}{100}\)
MgCO3 + 2HCL \(\rightarrow\) MgCL2 + CO2 + H2O
\(\dfrac{a}{84}\)-----------------------------------\(\dfrac{a}{84}\)
theo pthh:
n CO2 ( cốc A ) < n CO2 ( cốc B )
=> m CO2 ( cốc A ) < m CO2 ( cốc B )
=> m cốc A sau phản ứng > m cốc B sau phản ứng
- Trường hợp 2 : HCL thiếu
Có:
n HCl ( cốc A ) = n HCl ( cốc B )
=> n CO2 ( cốc A ) = n CO2 ( cốc B )
=> m CO2 ( cốc A ) = m CO2 ( cốc B )
Đúng 2
Bình luận (0)
Trên 2 đĩa cân thăng bằng có 2 cốc, cốc 1 chứa dd HCl và cốc 2 chứa dd H2SO4( đặc nóng). Người ta cho vào cốc 1 a gam CaCO3 vào cốc 2 b gam Cu.
a) Có thể tìm tỉ lệ a/b sao cho sau 1 thời gian 2 đĩa cân vẫn trở lại thăng bằng đc không?
b) Nếu ta cho a gam CaCO3 vào cốc 2 và b gam Cu vào cốc 1 thì để cho cân thăng bằng tỉ lệ a/b phải là bao nhiêu?
a) a(g) vào cốc CaCO3 xảy ra phản ứng:
\(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\)
b(g) vào cốc Cu xảy ra phản ứng:
\(Cu+H_2SO_4\rightarrow CuSO_4+SO_2+2H_2O\)
- Ở cốc 1 khối lượng tăng lên là (56/100)a. Ở cốc b khối lượng không thay đổi nên không thể xác định tỉ lệ a/b
b) \(CaCO_3+H_2SO_4\rightarrow CaSO_4+CO_2+2H_2O\)Cu vào cốc 1 không phản ứng.
Ở cốc 2, khối lượng tăng lên là: (56/100)a(g), cốc 2 tăng lên b(g)
Để cân thăng bằng thì (56/1000a=b=>a/b=100/56
Đúng 0
Bình luận (0)
Trên 2 đĩa cân thăng bằng có 2 cốc, cốc 1 chứa dd HCl và cốc 2 chứa dd H2SO4( đặc nóng). Người ta cho vào cốc 1 a gam CaCO3 vào cốc 2 b gam Cu.
a) Có thể tìm tỉ lệ a/b sao cho sau 1 thời gian 2 đĩa cân vẫn trở lại thăng bằng đc không?
b) Nếu ta cho a gam CaCO3 vào cốc 2 và b gam Cu vào cốc 1 thì để cho cân thăng bằng tỉ lệ a/b phải là bao nhiêu?

















